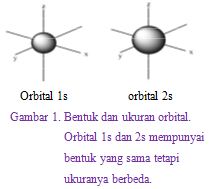
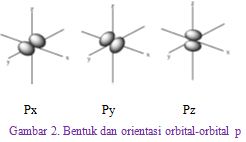
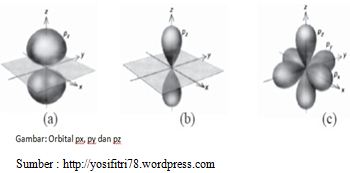
Setiap orbital mempunyai ukuran, bentuk, dan arah orientasi ruang yang ditentukan oleh bilangan kuantum n, l, dan m. Orbital-orbital tersebut bergabung membentuk suatu subkulit dan subkulit bergabung membentuk kulit atau tingkat energi.
untuk melihat videonya silahkan kunjungi alamat berikut ini http://www.youtube.com/watch?v=K-jNgq16jEY
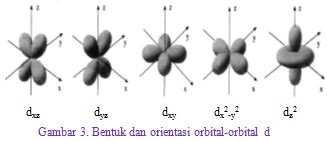
Sebagaimana ditunjukkan dalam Gambar 3. Salah satu orbital d, yaitu orbital dz2 , mempunyai bentuk yang berbeda dari 4 orbital d lainya. Meski bentuknya berbeda, kelima orbital d tersebut mempunyai tingkat energi yang sama
subkulit dengan nilai l yang lebih besar, yaitu subkulit f, g, dan seterusnya, mempunyai jumlah, bentuk serta orientasi orbital yang lebih rumit. Namun demikian, hal tersebut tidak terlalu penting untuk dipahami, antara lain karena orbital-orbital tersebut jarang digunakan dalam pembentukan ikatan kimia.
Jika anda telah memahami pengertian bilangan kuantum dan bentuk orbital silahkan pelajari contoh soal dan cobalah mengerjakan latihan soal.
Semangaaaatttttttt 🙂 jika anda mendapatkan nilai yang kurang memuaskan cobalah terus sampai anda berhasil mendapatkan nilai yang baik, kegagalan adalah awal dari keberhasilan 🙂
Jika anda telah berhasil mendapatkan nilai yang baik, silahkan lanjut ke materi selanjutnya yaitu Konfigurasi Elektron pada Atom.





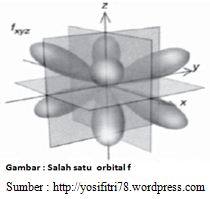
Kenapa d video tidak ada orbita f nya?